|
3
|
Bilangan oksidasi fosfor paling rendah terdapat pada senyawa …..
|
|
A
|
PH4Br
|
|
B
|
POBr3
|
|
C
|
PF3
|
|
D
|
PCl5
|
|
E
|
Ca3(PO4)2
|
|
4
|
Di antara setengah reaksi di bawah ini yang merupakan reaksi oksidasi adalah …..
|
|
A
|
Mg2+ 🡪 Mg
|
|
B
|
ClO3– 🡪 Cl–
|
|
C
|
SO2 🡪 SO42-
|
|
D
|
H2O2 🡪 H2O
|
|
E
|
HNO3 🡪 NO
|
|
5
|
Reaksi di bawah ini yang bukan merupakan reaksi redoks adalah …..
|
|
A
|
SnCl2 + I2 + 2HCl 🡪 SnCl4 + HI
|
|
B
|
H2 + Cl2 🡪 2HCl
|
|
C
|
CuO + 2HCl 🡪 CuCl2 + H2O
|
|
D
|
Cu2O + CO 🡪 2Cu + CO2
|
|
E
|
Fe2O3 + 3H2 🡪 2Fe + 3H2O
|
|
6
|
Pada reaksi : 2NH4+ + 6NO3– + 4H+ 🡪 6NO2 + N2 + 6H2O, zat pereduksi adalah …..
|
|
A
|
N2
|
|
B
|
NO2
|
|
C
|
H+
|
|
D
|
NO3–
|
|
E
|
NH4+
|
|
7
|
Reduksi satu mol ion BrO3– menjadi ion Br– membutuhkan elektron sebanyak …..
|
|
A
|
2 mol
|
|
B
|
3 mol
|
|
C
|
4 mol
|
|
D
|
5 mol
|
|
E
|
6 mol
|
|
8
|
Perhatikan reaksi redoks berikut : Sn(aq) + a HNO3(aq) 🡪 b SnO2(aq) + c NO2(g) + d H2O(l). harga koefisien a, b, c, dan d adalah …..
|
|
A
|
1, 4, 2, dan 4
|
|
B
|
1, 4, 4, dan 2
|
|
C
|
4, 2, 1, dan 4
|
|
D
|
4, 1, 4, dan 2
|
|
E
|
4, 1, 3, dan 4
|
|
9
|
Suatu reaksi redoks : a Br2 + b OH– 🡪 c BrO3– + dBr– + e H2O. Harga a, b, c, d, dan e agar setara berturut turut …..
|
|
A
|
3, 6, 1, 5, dan 3
|
|
B
|
3, 6, 5, 1, dan 3
|
|
C
|
6, 1, 5, 3, dan 3
|
|
D
|
6, 1, 3, 5, dan 3
|
|
E
|
1, 5, 3, 6, dan 3
|
|
10
|
Berikut adalah tiga senyawa yang mengandung unsur oksigen yaitu nitrogen monoksida, karbon dioksida, dan diklorooksida. Bilangan oksidasi unsur nitrogen, karbon, dan klorin pada senyawa tersebut berturut-turut adalah ….
|
|
A
|
+1; +2 ; +3
|
|
B
|
+1; +3 ; +2
|
|
C
|
+2; +4 ; +1
|
|
D
|
+2; +3 ; +1
|
|
E
|
+3; +4 ; +3
|
|
11
|
Perhatikan gambar rangkaian sel Volta berikut!
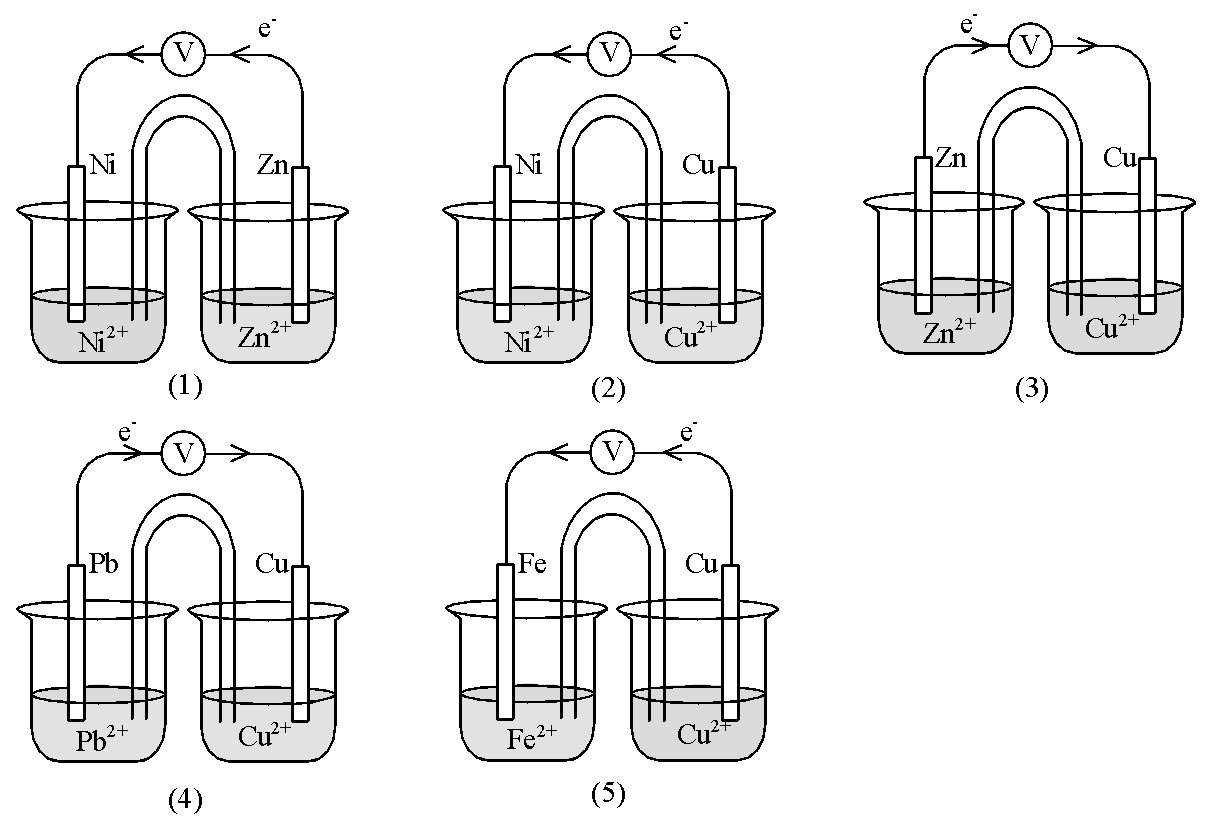
Nomor gambar, notasi sel, harga E0 sel yang tepat adalah ….
|
|
A
|
Nomor 1, Zn|Zn2+||Ni2+|Ni, harga E0 sel positif
|
|
B
|
Nomor 2, Cu|Cu2+||Ni2+|Ni, harga E0 sel positif
|
|
C
|
Nomor 3, Zn|Zn2+||Cu|Cu2+, harga E0 sel positif
|
|
D
|
Nomor 4, Pb|Pb2+||Cu|Cu2+, harga E0 sel positif
|
|
E
|
Nomor 5, Fe2+|Fe||Cu|Cu2+, harga E0 sel positif
|
|
12
|
Diketahui potensial elektroda:
F2(g) + 2e → 2F–(aq) Eo = +2,87 volt
Cl2(g) + 2e → 2Cl–(aq) Eo = +1,36 volt
Br2(g) + 2e → 2Br–(aq) Eo = +1,06 volt
I2(g) + 2e → 2I–(aq) Eo = +0,54 volt
Harga potensial reaksi : F2(g) + 2Cl–(aq) → Cl2(g) + 2F–(aq) adalah …
|
|
A
|
1,51 volt
|
|
B
|
1,90 volt
|
|
C
|
2,42 volt
|
|
D
|
3,41 volt
|
|
E
|
3,39 volt
|
|
13
|
Diketahui data dari Eo reduksi beberapa ion logam:
Eo Sn2+ = – 0,14 volt
Eo Mg2+ = – 2,37 volt
Eo Cu2+ = + 0,34 volt
Eo Fe2+ = – 0,44 volt
Eo Ni2+ = – 0,25 volt
Eo Pb2+ = – 0,13 volt
Logam yang dapat mencegah terjadinya korosi besi secara katodik adalah …..
|
|
A
|
Mg
|
|
B
|
Cu
|
|
C
|
Sn
|
|
D
|
Ni
|
|
E
|
Pb
|
|
14
|
Diketahui :
Cu2+(aq) + 2e– → Cu(s) Eo = + 0,34 volt
Fe3+(aq) + e– → Fe2+(s) Eo = + 0,77 volt
Pb2+(aq) + 2e– → Pb(s) Eo = – 0,13 volt
Cu2+(aq) + e– → Cu+(s) Eo = + 0,15 volt
Berdasarkan data tersebut, reaksi yang tidak dapat berlangsung adalah …
|
|
A
|
Fe3+(aq) + Pb(s) → Fe2+(aq) + Pb2+(aq)
|
|
B
|
Cu2+(aq) + Pb(s) → Cu+(aq) + Pb2+(aq)
|
|
C
|
Pb2+(aq) + Cu(s) → Pb(aq) + Cu2+(aq)
|
|
D
|
Fe3+(aq) + Cu(s) → Fe2+(aq) + Cu2+(aq)
|
|
E
|
Fe3+(aq) + Cu+(s) → Fe2+(aq) + Cu2+(aq)
|
|
15
|
Proses korosi / oksidasi paling mudah terjadi pada logam …..
|
|
A
|
Pt
|
|
B
|
Ni
|
|
C
|
Fe
|
|
D
|
Cr
|
|
E
|
Zn
|
|
16
|
Pernyataan yang benar mengenai sel elektrokimia adalah…..
|
|
A
|
Pada sel volta listrik diubah menjadi energi kimia
|
|
B
|
Pada sel volta katoda merupakan kutub negatif
|
|
C
|
Pada elektrolisis oksidasi berlangsung di katoda
|
|
D
|
Pada sel elektrolisis reaksi kimia berlangsung tidak spontan
|
|
E
|
Batu batere merupakan contoh dari sel elektrolisis
|
|
17
|
Elektrolisis yang menghasilkan gas oksigen pada anoda adalah …..
|
|
A
|
NH3(l)
|
|
B
|
Na2SO4(aq)
|
|
C
|
NaCl(l)
|
|
D
|
HCl(aq)
|
|
E
|
KBr(l)
|
|
18
|
Peristiwa yang terjadi di elektroda negatif pada elektrolisis larutan Na2SO4 menggunakan elektrode grafit adalah …..
|
|
A
|
Terbentuk logam natrium
|
|
B
|
Terbentuk gas oksigen
|
|
C
|
Larutan bersifat asam
|
|
D
|
Larutan bersifat basa
|
|
E
|
Terbentuk gas SO2
|
|
19
|
Pada elektrolisis lelehan NaCl, pada katoda dan anoda dihasilkan …..
|
|
A
|
H2 dan Cl2
|
|
B
|
Na dan Cl2
|
|
C
|
Na dan O2
|
|
D
|
H2 dan O2
|
|
E
|
Na dan H2
|
|
20
|
Pada elektrolisis lelehan MgCl2 jika di anoda dihasilkan 5,6 L gas Cl2( STP), maka muatan listrik yang digunakan …..Faraday
|
|
A
|
0,05
|
|
B
|
0,1
|
|
C
|
0,5
|
|
D
|
1
|
|
E
|
2
|







